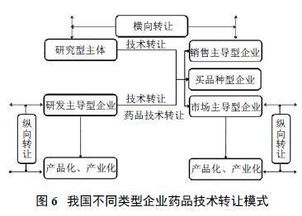
中國藥品注冊審評制度經歷了一系列深刻改革,旨在鼓勵創新、提高藥品質量、加速新藥上市。這一系列改革,如上市許可持有人制度(MAH)的全面實施、優先審評審批通道的建立、以及與國際接軌的審評標準提升,不僅重塑了藥品研發與注冊的生態,也為藥品技術轉讓這一傳統業務領域帶來了全新的發展格局。技術轉讓,作為藥品生命周期中優化資源配置、加速產品商業化的重要環節,正站在機遇與挑戰并存的關鍵路口。
一、 改革帶來的歷史性機遇
- 制度松綁,激活市場活力:MAH制度的推行是核心機遇。它實現了藥品上市許可與生產許可的“解綁”,允許研發機構、科研人員等持有藥品批文,并委托生產企業進行生產。這極大地降低了技術持有方進行轉讓的門檻和風險,使得更多實驗室階段的創新成果能夠通過技術轉讓路徑,快速找到具備生產能力和市場渠道的合作伙伴,實現產業化。技術轉讓不再必然伴隨生產線的整體出售,變得更加靈活多樣。
- 價值重估,創新成為硬通貨:審評改革強調臨床價值,對真正具有創新性、能夠解決未滿足臨床需求的藥品開辟了優先審評、突破性治療藥物等加速通道。這使得具有突出臨床優勢的早期項目或專利技術在轉讓市場上的價值顯著提升。買方更愿意為具有明確創新點和市場潛力的技術支付溢價,激勵了源頭創新,也促使技術轉讓更早地介入研發鏈條。
- 路徑清晰,降低轉讓不確定性:改革后的審評流程更加透明、可預期,技術要求與國際逐步接軌。這使得在技術轉讓過程中的盡職調查更有依據,對技術的成熟度、合規性、知識產權狀況的評估更為準確。清晰的法規框架降低了交易雙方因政策變動帶來的不確定性,有利于達成更公平、穩定的轉讓協議。
- 生態繁榮,催生專業服務需求:隨著交易活躍度提升,圍繞藥品技術轉讓的第三方專業服務市場,如法規咨詢、價值評估、知識產權服務、交易中介等,迎來發展契機。一個更加專業、細分的服務體系能夠進一步促進技術的高效流轉。
二、 面臨的全新挑戰
- 標準提升,對技術質量要求更嚴苛:與國際接軌的審評標準,意味著轉讓的技術必須滿足更高的藥學、臨床和質量一致性評價要求。一些基于舊標準開發、數據不夠完整或質量體系有缺陷的技術,其轉讓價值將大打折扣甚至無法轉讓。這對技術持有方的研發質量和數據管理能力提出了嚴峻挑戰。
- 責任明確,MAH制度下的風險管控:在MAH制度下,上市許可持有人對藥品的全生命周期質量承擔主體責任。對于技術受讓方(尤其是成為MAH的一方)而言,如何確保對受托生產企業的有效管理,如何建立覆蓋全鏈條的質量管理體系,是全新的課題。技術轉讓協議中關于質量責任、藥物警戒、上市后研究等責任的劃分必須極其清晰。
- 競爭加劇,對綜合研判能力要求更高:政策鼓勵創新導致源頭項目爭奪激烈,優質技術成為稀缺資源。潛在受讓方(如大型藥企)的選擇也更多,其眼光更加挑剔。技術轉讓的成功不再僅依賴于“有批文”,更取決于對技術臨床優勢、市場潛力、專利布局、后續開發成本與風險的精準綜合研判。這對交易雙方的戰略眼光和專業能力構成了挑戰。
- 過程復雜,全鏈條整合需求凸顯:現代藥品技術轉讓往往不是簡單的“紙面資料”移交,而可能涉及生產工藝的轉移與驗證、質量標準銜接、供應鏈重構、注冊檔案的變更與申報等一系列復雜活動。這要求交易雙方具備強大的項目管理和跨部門整合能力,任何環節的疏漏都可能導致轉讓失敗或成本超支。
三、 展望與應對之道
面對機遇與挑戰,藥品技術轉讓的參與者需要積極適應新環境:
- 對于技術持有方:應注重研發的合規性與數據完整性,加強知識產權保護與布局,在研發早期就引入商業化思維,提前準備符合新規的技術轉讓資料包。
- 對于技術受讓方:需建立科學的技術評估體系,不僅關注眼前批文,更要評估技術的長期開發潛力和MAH責任下的風險管控能力,加強自身對委托生產的管理體系建設。
- 對于行業整體:應倡導更加規范、誠信的交易文化,發展專業的中介評估機構,利用合同明確界定各環節權責利,共同構建一個高效、透明、風險可控的藥品技術轉讓市場。
中國藥品注冊審評制度改革如同一股強勁的東風,既為藥品技術轉讓打開了更廣闊的空間,也設定了更高的航行標準。唯有那些能夠深刻理解政策內涵、精準把握技術價值、并具備卓越執行力的企業與機構,才能在這場變革中乘風破浪,實現技術與資本、研發與市場的成功對接,最終惠及患者,推動中國醫藥產業的高質量發展。